單細胞轉(zhuǎn)錄組測序(Single-cell RNA-sequencing, scRNA-seq)是在單個細胞水平對mRNA進行高通量測序的一項新技術(shù)����,原理是將分離的單個細胞中微量的mRNA通過高效擴增后再進行高通量測序����。單細胞轉(zhuǎn)錄組測序能夠有效解決組織樣本細胞異質(zhì)性以及常規(guī)RNA-seq被掩蓋的細胞群內(nèi)的轉(zhuǎn)錄組異質(zhì)性難題����,有助于發(fā)現(xiàn)新的稀有細胞類型,并深入了解細胞生長過程中的表達調(diào)控機制����。
基于10x Genomics最新Chromium系統(tǒng)利用油包水的微反應(yīng)體系�����,通過序列標簽(cell barcode和UMI)區(qū)別群體中的不同細胞和轉(zhuǎn)錄本��,獲得單細胞水平的基因表達譜����,可實現(xiàn)數(shù)千甚至上萬個單細胞群體分析,解決常規(guī)scRNA-seq方法在通量或擴展性方面存在的不足�,為單細胞研究開拓新的思路。
單細胞轉(zhuǎn)錄組測序技術(shù)優(yōu)勢
通量高����,一次可以同時測8個樣本��,每個樣本最多可以測10000個細胞
周期短�,6分鐘內(nèi)完成上萬個細胞封裝��,一天之內(nèi)完成細胞懸液制備����、單細胞捕獲、擴增以及建庫
捕獲效率高����,單個細胞捕獲效率高達65%
應(yīng)用范圍廣,動物細胞���、植物細胞均可以進行單細胞測序�,廣泛應(yīng)用于腫瘤細胞異質(zhì)性����、免疫細胞群體檢測以及胚胎發(fā)育等研究
技術(shù)原理
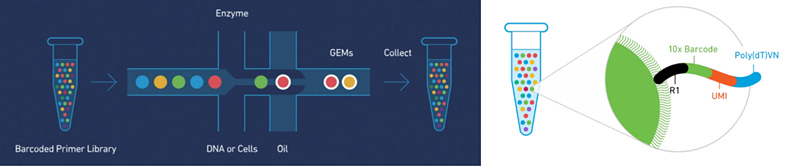
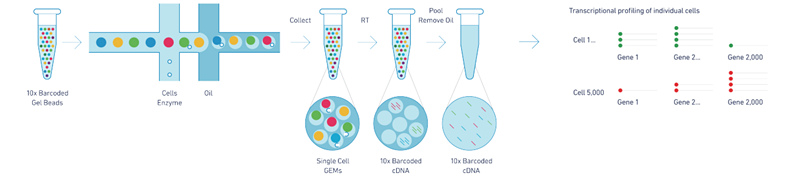
利用8通道的微流體“雙十字”交叉系統(tǒng),將含barcode的凝膠珠(Gel Beads)����、細胞和酶的混合物���、油三者混合,形成GEMs�����。
GEMs形成后�,細胞裂解,凝膠珠自動溶解釋放大量barcode序列���,隨后mRNA逆轉(zhuǎn)錄產(chǎn)生帶有Barcode和UMI信息的cDNA����,再構(gòu)建標準測序文庫��。
建庫流程
案例展示
案例一 通過10× genomics單細胞轉(zhuǎn)錄組測序繪制肺癌腫瘤微環(huán)境圖譜
Phenotype molding of stromal cells in the lung tumor microenvironment
研究背景
腫瘤周圍的組織�����、免疫細胞�、血管和細胞外基質(zhì)共同形成的腫瘤微環(huán)境對腫瘤的生長和侵襲至關(guān)重要����,本研究試圖通過單細胞轉(zhuǎn)錄組測序揭示肺癌腫瘤微環(huán)境的特征�����。
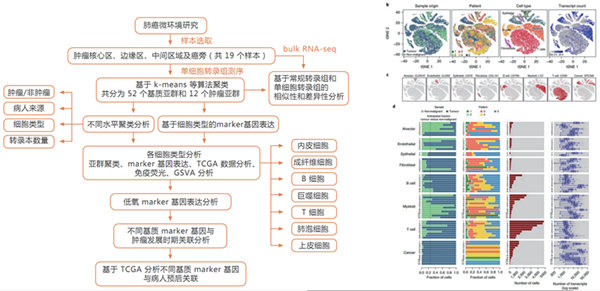
技術(shù)路線
研究結(jié)果
文章共選取5例共19個樣本��,通過10×genomics單細胞轉(zhuǎn)錄組測序探索基質(zhì)細胞的亞群分類��、基因功能(信號通路)�、關(guān)鍵marker基因和臨床預(yù)后���。共鑒定出52個基質(zhì)細胞亞群�����,反映了腫瘤微環(huán)境復(fù)雜性��。對基質(zhì)細胞的marker基因做生存曲線��,發(fā)現(xiàn)這些marker基因可以作為肺癌預(yù)后診斷的潛在標志物�����。
單細胞轉(zhuǎn)錄組測序常見問題
1. 為什么每個樣品需要那么多的細胞量?
答:細胞在上機之前��,需要對進行一系列的質(zhì)檢���,質(zhì)檢過程需要用掉部分細胞�。
2. 如何檢測細胞活性?
答:可以使用臺盼藍染色��,用顯微鏡觀察細胞活性����。
3. 植物細胞能做單細胞測序嗎?
答:植物細胞可以做單細胞測序,但需要注意兩點:1. 需要注意細胞大小��,10× genomics的適用對象是直徑小于40 nm的細胞��。2. 植物細胞含有細胞壁��,細胞壁對后續(xù)裂解有影響�����,所以需要用纖維素酶等消化細胞壁���,制成原生質(zhì)體。
4. 單細胞測序需要和常規(guī)轉(zhuǎn)錄組一樣設(shè)置重復(fù)嗎?
答:單細胞測序的目的是分離群體細胞中的不同亞群�����,表征這些亞群的特征,我們建議老師最好有實驗組和對照組��,但一般對生物學(xué)重復(fù)沒有要求�。
免責(zé)聲明:部分圖片來源于網(wǎng)絡(luò),如有侵權(quán)請聯(lián)系刪除��!